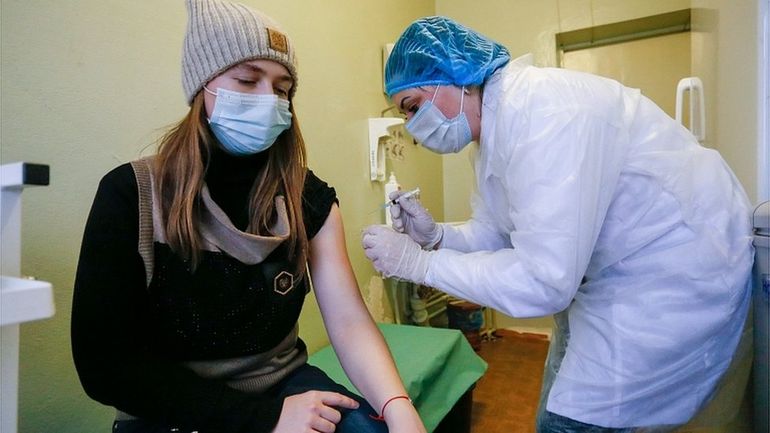
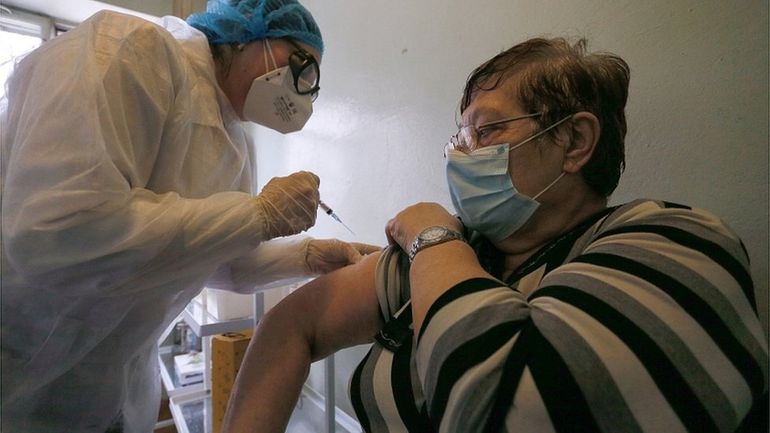
Авторитетный научный журнал Lancet опубликовал результаты третьей фазы клинических испытаний российской вакцины "Спутник V", разработанной исследовательским Центром имени Гамалеи.
Согласно предварительным данным, эффективность вакцины против заражения коронавирусом SARS-CoV-2 составила 91,6%. Как подчеркивают ученые, такая же эффективность была и в группе людей старше 60 лет. Как заявил на брифинге, посвященном публикации, глава центра Гамалеи Александр Гинцбург, ученые пришли к выводу, что иммунитет после "Спутника" может сохраняться "по крайней мере два года и более".
По словам главы РФПИ Кирилла Дмитриева, вакцина эффективна против обнаруженных в Великобритании и ЮАР новых штаммов коронавируса.
По данным исследователей, "Спутник" "на 100% защищает" от среднего и тяжелого течения Covid-19. Во время исследования было несколько смертей добровольцев, но с введением вакцины они не связаны, говорится в статье Lancet.
Эффективность
Согласно промежуточным результатам исследования, проведенного на 20 тысячах человек, вакцина показала эффективность 91,6% против Covid-19.
Из группы добровольцев, состоящей из 14 964 человек, которые получили укол настоящей вакцины, в итоге заболели 16 человек, или 0,1% тех, кому ввели препарат. В группе плацебо, в которую вошли 4902 человека, заболели 62 человека - 1,3% тех, кому ввели физраствор. Это число заболевших зафиксировали через 21 день после получения первой дозы препарата.
ПЦР-тесты на коронавирус исследуемым проводили при первичном скрининге и перед введением второй дозы, сообщается в статье. Тест также проводили, если участники сообщали о симптомах ОРВИ.
/nginx/o/2021/02/02/13609478t1hffa8.jpg)
/nginx/o/2019/10/16/12659746t1hee98.png)